文章来源:https://www.lanqiaopf.com/ 作者:未知 发布时间:2022-11-09 浏览次数:121
一、无菌医疗器械生产中应当采用使细菌污染降至最低限的生产技术,以保证医疗器械不受污染或能有效排除污染。
二、主要与创面接触的医疗器械或单包装出厂的配件,其(不清洗)零部件的加工、末道清洗、组装、初包装及其封口等生产区域应不低于十万级洁净度级别。
三、主要与组织和组织液接触的无菌医疗器械或单包装出厂的配件,其(不清洗)零部件的加工、末道清洗、组装、初包装及其封口等生产区域应不低于十万级洁净度级别。
四、主要与血液接触的无菌医疗器械或单包装出厂的配件,其(不清洗)零部件的加工,末道清洗、组装、初包装及其封口等生产区域应不低于十万级洁净度级别。
五、与人体损伤表面和粘膜接触的无菌医疗器械或单包装出厂的(不清洗)零部件的加工、末道精洗、组装、初包装及其封口均应在不低于十万级洁净室(区)内进行。生产企业应对与人体损伤表面接触的无菌医疗器械或单包装出厂的(不清洗)零部件的加工、末道精洗、组装、初包装及其封口所要求的环境进行必要的验证、确认。
六、与无菌医疗器械的使用表面直接接触、不清洗即使用的包装材料,生产企业应采取措施,使包装材料达到相应的洁净程度和无菌要求,并经过验证,若包装材料不与无菌医疗器械使用表面直接接触,应在不低于十万洁净室(区)内生产。

七、对于有要求或采用无菌操作技术加工的无菌医疗器械(包括医用材料),应在万级下的局部百级洁净室(区)内进行生产。
八、洁净工作服清洗、干燥和穿洁净工作服室、专用工位器具的末道清洗与消毒的区域的空气洁净度级别可低于生产区一个级别。无菌工作服的整理、灭菌后的贮存应在万级洁净室(区)内。
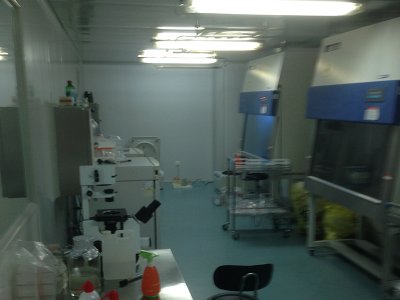
 医疗器械净化车间的设计参数及方案
医疗器械净化车间的设计参数及方案
根据相关规范要求,无菌 医疗器械净化车间 、药品生产车间、医学生物学实验室、手术室等。要求建造符合相...
TIME:2022-05-31
济南兰桥净化工程有限公司
统一客户咨询电话
186-6074-8817
官方网址:https://www.lanqiaopf.com/
联系地址:济南市华山西路8号